In dit experiment is er een verwarmingselement in een met water gevulde maatbeker gestopt. Elke minuut is de temperatuur van het water gemeten. Deze metingen zijn opgeslagen in tempmetingen.csv.
Verder is gegeven dat:
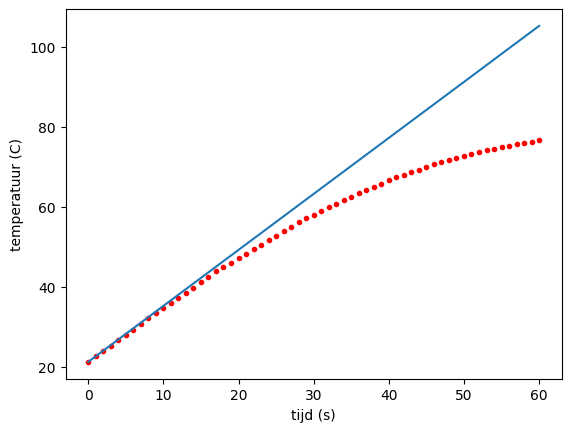
Het moge duidelijk zijn dat er water is ‘verdwenen’. Ook is de eindtemperatuur van het water niet gelijk aan een proces waarbij verdamping en eventuele warmteverliezen niet meegenomen worden.
import numpy as np
import matplotlib.pyplot as plt
from scipy.optimize import curve_fit
data = np.loadtxt(r"C:\Users\fiene\OneDrive\Project Q1 2025\IP Q2\Thermo project Q2 Fiene en Thomas\Fiene-en-Thomas\Content\Labs\tempmetingen-0203356cbb854ce862d0304505c4ede5.csv", delimiter=';', skiprows=1)
m_mb = 0.8208
m_mw1 = 1.2929
m_mw2 = 1.2749
m_w1 = m_mw1 - m_mb
m_w2 = m_mw2 - m_mb
dm = m_w2 - m_w1
t_min = data[:,0]
t = t_min*60
T = data[:,1]
T0 = T[0]
def model(t, T0, k):
return T0 + k*t
c= 4184.0
P = None
if P is None:
coef = np.polyfit(t[:3], T[:3], 1)
slope = coef[0]
P = c*m_w1*slope
T_exp = T0 + (P / (c* m_w1)) *t
plt.figure()
plt.plot(t_min, T, 'r.')
plt.plot(t_min, T_exp)
plt.xlabel('tijd (s)')
plt.ylabel('temperatuur (C)')
plt.show()
# Opdracht 2
# eindtemperatuur en totale tijd
Te = T[-1]
t_tot = t[-1] # al in seconden
dT = Te - T0
Q_tot = P * t_tot #in Joule
Q_water = m_w1 * c * dT # c is al 4184 J/(kg K)
c_glass = 840.0 # J/(kg K), soortelijke warmte glas (aangenomen)
Q_beker = m_mb * c_glass * dT
Q_rest = Q_tot - (Q_water + Q_beker)
L_v = 2.26e6 # J/kg
if Q_rest > 0:
m_verdampt_theor = Q_rest / L_v # kg
else:
m_verdampt_theor = 0.0
dm_meet = m_w1 - m_w2 # kg
print("=== Energetische analyse ===")
print(f"vermogen P = {P:.1f} W")
print(f"totale tijd = {t_tot:.1f} s")
print(f"Q_tot (toegevoegd) = {Q_tot:.0f} J")
print(f"Q_water (opwarming) = {Q_water:.0f} J")
print(f"Q_beker (opwarming) = {Q_beker:.0f} J")
print(f"Q_rest (voor verdamping)= {Q_rest:.0f} J")
print(f"m_verdampt_theor = {m_verdampt_theor*1000:.2f} g")
print(f"m_verdampt_gemeten = {dm_meet*1000:.2f} g")
=== Energetische analyse ===
vermogen P = 46.1 W
totale tijd = 3600.0 s
Q_tot (toegevoegd) = 165922 J
Q_water (opwarming) = 109430 J
Q_beker (opwarming) = 38197 J
Q_rest (voor verdamping)= 18296 J
m_verdampt_theor = 8.10 g
m_verdampt_gemeten = 18.00 g
Opdracht 2
Uit de berekeningen blijkt dat het verwarmingselement in totaal 165922 J aan energie toevoegt. Daarvan gaat ongeveer 109430 J naar het opwarmen van het water en 38197 J naar het opwarmen van de maatbeker. Er blijft dan 18296 J over voor verdamping.
Met die hoeveelheid energie zou er theoretisch ongeveer 8,10 g water moeten verdampen. In werkelijkheid is er 18,00 g verdwenen.
De gemeten verdamping is dus veel groter dan wat je op basis van de energie zou verwachten. Dat betekent dat er tijdens het experiment veel warmte verloren gaat naar de omgeving, waardoor het model (alle energie → opwarming + verdamping) niet klopt.
Opdracht 3
Het experiment wijkt af van de theorie, vooral omdat er veel warmte verloren gaat. Een belangrijke verbetering zou zijn om de maatbeker beter te isoleren, bijvoorbeeld door er isolatiemateriaal omheen te doen, zodat er minder warmte naar de omgeving verdwijnt. Het zou ook helpen om het vermogen van het verwarmingselement nauwkeuriger te bepalen door spanning en stroom te meten, of door een element te gebruiken waarvan het vermogen al bekend is. Daarnaast zou het experiment betrouwbaarder worden als de massa tijdens het verwarmen continu wordt gemeten op een weegschaal, zodat je precies kunt zien hoeveel water er werkelijk verdampt. Verder is het slim om de temperatuursensor eerst te kalibreren en wat vaker te meten, zodat de temperatuurgegevens kloppen en de stijging realistischer is. Tot slot kun je het hele experiment het beste meerdere keren uitvoeren om te controleren of de resultaten steeds ongeveer gelijk zijn. Daarmee krijg je een beter beeld van de onzekerheid in je metingen.